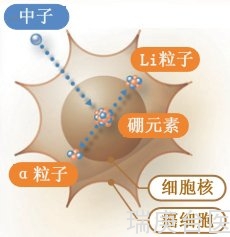
硼中子俘获疗法(BNCT)是基于硼-10(天然元素硼的非放射性成分)被低能量(0.025 eV)热中子辐照时发生的核俘获和裂变反应。这导致产生高线性能量转移(LET)粒子(4He)和反冲锂-7(7Li)原子核。
为了获得成功,必须有选择地向所有肿瘤细胞输送足够数量的10B(~20μg/g或~109个原子/细胞),并吸收足够的热中子,以通过10B(n,α)7Li捕获反应造成致命破坏。这些高能粒子的破坏作用于含硼的细胞,由于它们在组织中的通路长度很短(5–9μm),因此从理论上讲BNCT提供了一种选择性地破坏恶性细胞并保护邻近正常细胞的方法。临床兴趣的BNCT主要集中在高级别胶质瘤,病人复发的肿瘤的头部和颈部地区的常规治疗失败。BNCT主要是一种生物化学疗法,而不是物理靶向类型的放射治疗,因此,它应该有可能选择性地破坏分散在正常组织中的肿瘤细胞,只要有足够数量的10B和热中子被送到肿瘤部位。
BNCT含硼递送剂的研究始于大约50年前,研究了大量低分子量硼化合物,并由此产生了递送剂。BNCT给药重要的要求是:1.低毒,组织摄取正常,肿瘤:正常组织,肿瘤:血液(T:Bl)硼浓度比为~3:2.)肿瘤硼浓度~20°g 10B/g肿瘤;3)在中子照射下,血液和正常组织相对快速清除,肿瘤持续存在。目前临床试验中仅使用的两种BNCT给药药物通常称为硼氢化钠(BSH),和硼苯丙氨酸或双酚或BPA。这两种试剂都不能完全满足上述标准,因此第三代掺杂一个或多个多面体硼烷阴离子或碳硼烷的试剂已被研究。随着新合成技术的发展和人们对有效含硼剂及其输送方式的生化要求的提高,出现了许多新的含硼剂。开发这类制剂的主要挑战是需要有选择性的肿瘤细胞靶向和提供具有小正常组织毒性的治疗性硼水平。与其他解剖部位的恶性肿瘤相比,在正常大脑中对胶质母细胞瘤(GBM)细胞进行局部和有效的破坏是一个更大的挑战。这是由于一个额外的生物屏障——血脑屏障(BBB),以及胶质瘤细胞的高度浸润性和分子异质性造成的。
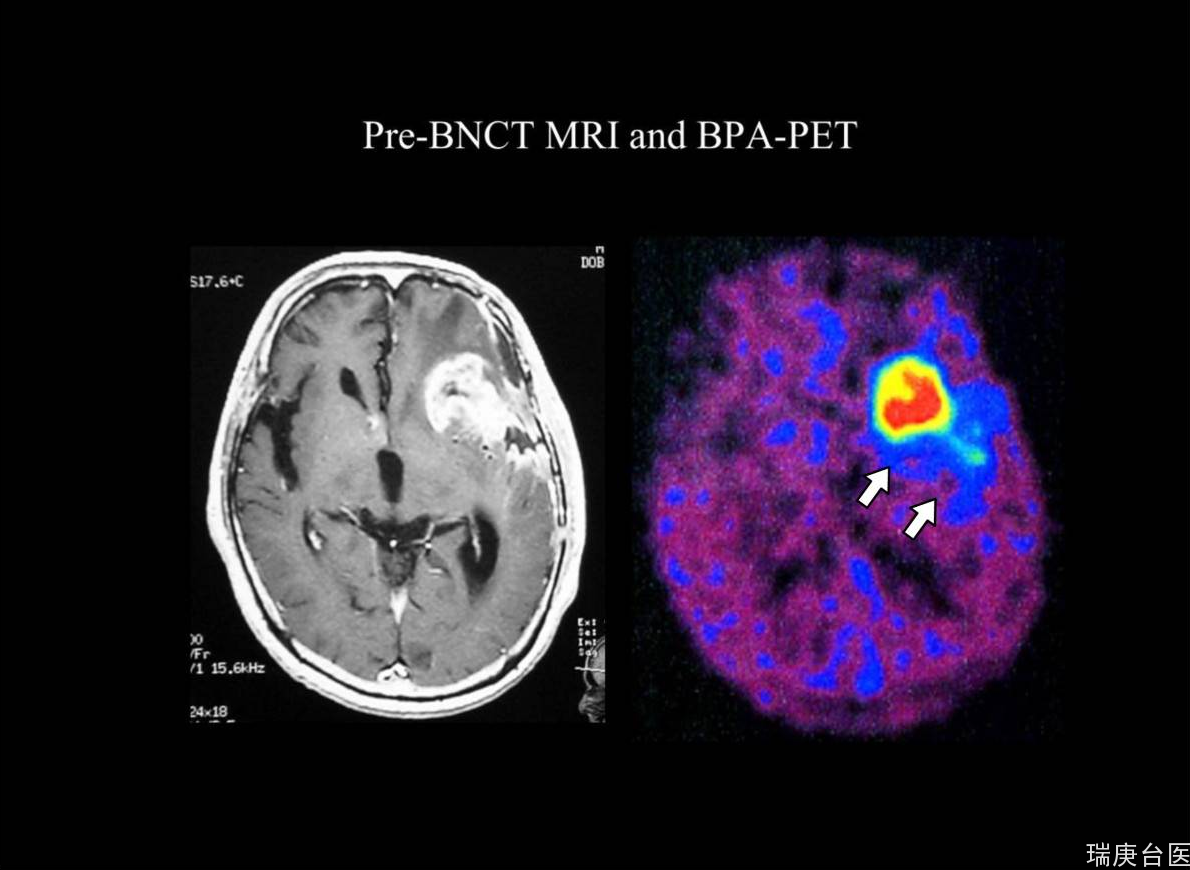
图示:典型胶质母细胞瘤患者的t1加权MRI造影增强和荧光标记的18 F-BPA-PET图像。
它可能在于为那些没有有效治疗方法的恶性肿瘤,无论是原发性的还是复发性的,填补一个空白。BNCT有哪些优势?
第一它具有选择性地向肿瘤输送高辐射剂量而向周围正常组织输送低得多的剂量的能力。这是一个重要的特点,使BNCT特别有吸引力的挽救治疗的病人谁已经接受了光子照射的耐受性。
第二与原发性和转移性脑肿瘤的立体定向放射外科相比,它具有更有效地靶向肿瘤的多中心沉积的潜力。
第三,尽管它可能只是治标不治本,但它可以产生显著的临床反应,正如几组治疗复发性、治疗难治性头颈癌患者的经验所证明的那样。在治疗原发性或复发性高级别胶质瘤患者中获得的临床结果,在改善临床结果方面已经取得了显著进展。
具体来说,增加双酚a的剂量并在更长的时间内给药,或者将BNCT疗法与光子增强疗法相结合,像在日本所做的那样,已经产生了迄今为止使用BNCT疗法治疗神经胶质瘤患者所获得的生存数据。
新型低分子量和高分子量硼制剂的开发及其释放的优化:
获得监管机构对这些新药物临床应用的批准,并在肿瘤切除前对患者进行生物分布研究;
确定合作努力的优先顺序,以比较和规范各中心之间的剂量处方,从而能够对更大的试验人群进行研究,并可能促进多机构或可能随机的临床试验;
改进在宏观和微观水平上确定输送到残留肿瘤体积的硼剂量的方法,以实现更精确的肿瘤剂量评估。
准备好与新的治疗方法竞争或互补。
胶质母细胞瘤是非常致命的原发性颅内肿瘤,总生存期为15-18个月, 2年生存率为 25% 。影响预后的因素包括年龄、神经功能状态、手术切除程度、分子生物学特性、放化疗等。目前手术切除是胶质母细胞瘤有效的治疗方法,可有效延长患者的生存期限。但是目前基于影像学的胶质母细胞瘤手术切除范围仍有争议。胶质母细胞瘤分为原发性和继发性。其亚型包括巨细胞型胶质母细胞瘤和胶质肉瘤,占神经上皮组织肿瘤的23%;可发生于任何年龄阶段,以45-65岁高发,30岁以下者鲜见;男性明显高于女性。
成都瑞庚医疗科技咨询有限公司
公司网址丨www.ruigeng.net
公司邮箱丨rg@ruigeng.net
洽询电话丨028-61985320
微信客服丨18982287599
微信公众号丨瑞庚台医

 微信扫码
微信扫码
 意见反馈
意见反馈
 热线电话
热线电话

 ivy-客服
ivy-客服