患者:男性
年龄:35岁左右
病症:复发性间变性少星形细胞瘤
治疗:BNCT与BV治疗
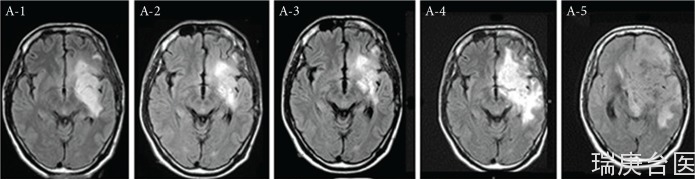
在接受BNCT和BV治疗之前,他抱怨说癫痫很难控制。治疗后,癫痫发作可以得到很好的控制,患者的核磁共振成像表现出改善。在BNCT之前、之后7个月和之后13个月,重复的双酚a正电子发射断层扫描分析分别得出了5.0、1.9和2.1的左/右比值,如图。不幸的是,核磁共振成像恶化了图1A-4和B-4,患者在BNCT手术后38个月死于肿瘤进展。患者接受了55个疗程的BV。突出的AE是全身疲劳和蛋白尿(CTCAE 2级)。
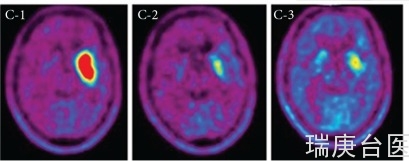
C-1到C-3显示了F-BPA-PET研究。
增强肿瘤病灶与正常脑(L/N)的比例分别为5.0 (C-1)、2.2 (C-2)和1.7 (C-3)。
A-1, B-1和C-1;真挚里之前。
A-2, B-2和C-2;BNCT后7个月。
A-3, B-3和C-3;BNCT后13个月。
B-4;BNCT后26.5个月。
B-5;BNCT后33个月。
这是该治疗方案出现的典型肿瘤复发。BV治疗可控制BRN,但BNCT后仍有肿瘤复发。据报道,维持性BV治疗的肿瘤复发似乎具有侵袭性。
复发性恶性胶质瘤的预后很差,并且还没有建立标准的治疗方法。自2002年以来,研究所已经应用了一种称为硼中子俘获疗法(BNCT)的肿瘤选择性粒子放射疗法,用于RMGs患者,并观察到良好的生存结果。
BNCT是一种以生物化学为目标的放射疗法,其基础是当非放射性硼-10(天然元素硼的一种成分)受到低能热中子照射时发生的核俘获和裂变反应,从而产生高能线性转移α粒子和反冲锂-7核。这些粒子在非常短的范围内释放,例如9微米,因此细胞毒性作用于含硼10的细胞。
含硼化合物可以通过几种机制在肿瘤细胞中选择性地积累。例如,与正常细胞相比,氨基苯丙氨酸(BPA)通过氨基酸转运蛋白增加的氨基酸代谢在肿瘤细胞中被选择性和优先积累。即使有了这种新颖和选择性的粒子放射疗法,放射损伤——主要是脑放射坏死(BRN)和症状性假进展(PSPd)——也经常发生,辐射损伤在RMG病例中尤其可能,因为在此类病例中,全剂量x光治疗(XRT)通常是治疗史的一部分。
在之前分析人类BRN手术标本的研究中,我们发现BRN中的水肿是由反应性星形胶质细胞中血管内皮生长因子的过度表达引起的。贝伐单抗(BV),一种抗血管内皮生长因子抗体,被用于治疗有症状的BRN。基于这些发现,我们使用了BV来试图控制症状性BRN和BNCT后出现的帕金森病。
有几份报告审查了在RMG使用再辐射的情况,并增加了BV,以防止辐射伤害并通过克服低氧介导的抗辐射机制来增强辐射的功效。文中,评估了这种治疗的可行性和有效性。
恶性胶质瘤仍然是神经肿瘤学中具侵袭性和破坏性的肿瘤之一。尽管进行了广泛的研究,治疗结果仍然不令人满意。诊断时,治疗通常包括神经外科切除,尽可能根治但不导致明显的发病率,然后是术后放射治疗。通过这种组合,获得了9-12个月的总存活率。近日,新的化疗方案被添加到这种治疗组合中。用替莫唑胺进行的放化疗使总存活时间显著延长至14.6个月。放射治疗同时应用ACNU/VM26可将总生存期延长至16.5个月。然而,几乎所有的格林-巴利综合征都会复发,局部衰竭是常见的复发模式。因此,局部控制是帮助提高格林-巴利综合征患者整体生存率的关键问题。
在大多数患者中,复发时的治疗选择是有限的。化疗是复发性胶质瘤常用的治疗方法。放射治疗作为复发性胶质瘤的一种治疗方法是有争议的。一般来说,在初步诊断后,手术后应用全剂量的辐射,再辐射与较高的BRN风险相关,其毒性大于其益处。
与单独使用BNCT相比,这种治疗方案中常见和突出的额外AE是蛋白尿。在这个系列中,蛋白尿的发生率和严重程度可能与BV总剂量有关。在文献中,只有两篇关于蛋白尿发生率与BV总剂量的关系的报道。Hayman SR报告了蛋白尿和BV的累积剂量之间有明显的关系,而Slusarz没有发现任何关系。已经有一些关于单剂量BV和蛋白尿之间的特殊关系的报道。研究人员报告,小剂量的BV (5 mg/kg,双周)方案仍然显示出对BRN的有效作用。因此,还需要进一步的临床试验来检验这种小剂量降低蛋白尿风险的潜力。此外,BV治疗的时间应该在BNCT后的一个月内开始,是在2周内,因为病例1在BNCT后1个月出现有症状的psPD,随后BV的增加又恢复了。
研究表明,硼中子捕获治疗和BV治疗能够很好地预防或控制BRN,延长OS和可接受的AE发生率。
成都瑞庚医疗科技咨询有限公司
公司网址丨www.ruigeng.net
公司邮箱丨rg@ruigeng.net
洽询电话丨028-61985320
微信客服丨18982287599
微信公众号丨瑞庚台医

 微信扫码
微信扫码
 意见反馈
意见反馈
 热线电话
热线电话

 ivy-客服
ivy-客服